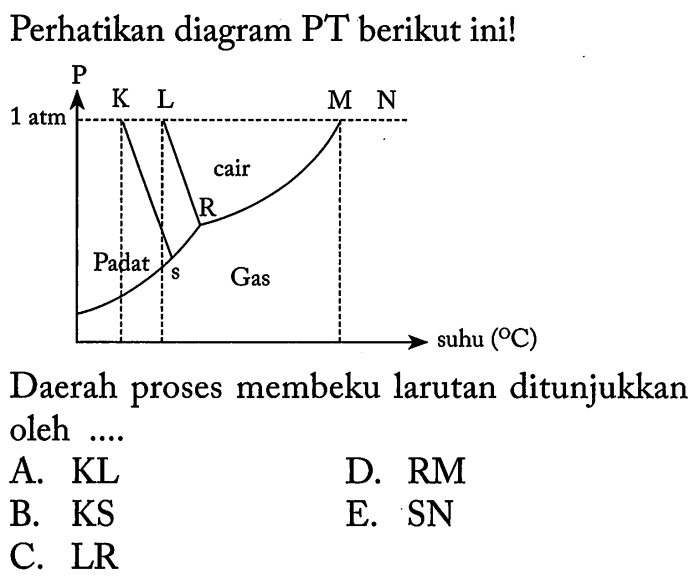
Dalam kimia, sifat koligatif larutan memainkan peran penting dalam memahami perilaku larutan dan aplikasinya dalam berbagai bidang. Sifat-sifat ini bergantung pada konsentrasi partikel terlarut, bukan identitas kimianya. Diagram fasa, yang menggambarkan hubungan antara suhu, tekanan, dan komposisi larutan, memberikan wawasan berharga tentang sifat koligatif ini.
Diagram fasa memberikan pemahaman visual tentang perubahan sifat fisik larutan, seperti titik beku, titik didih, dan tekanan osmotik, sebagai fungsi konsentrasi zat terlarut. Dengan memahami prinsip-prinsip yang mendasari sifat koligatif dan cara membaca diagram fasa, kita dapat memperoleh wawasan yang lebih dalam tentang perilaku larutan dan penerapannya dalam kehidupan sehari-hari dan industri.
Sifat Koligatif
Sifat koligatif adalah sifat larutan yang bergantung pada jumlah partikel terlarut, bukan pada jenis partikel terlarut. Sifat-sifat ini dipengaruhi oleh konsentrasi partikel terlarut, bukan identitas kimianya.
Jenis-jenis Sifat Koligatif
- Penurunan Tekanan Uap
- Kenaikan Titik Didih
- Penurunan Titik Beku
- Tekanan Osmotik
Diagram Fasa
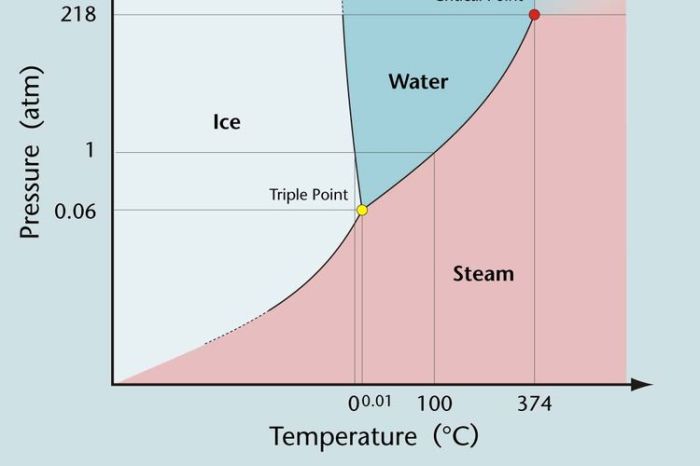
Diagram fasa merupakan representasi grafis dari kondisi kesetimbangan suatu sistem yang terdiri dari beberapa fase.
Dalam larutan, diagram fasa dapat digunakan untuk menggambarkan hubungan antara suhu, tekanan, dan konsentrasi larutan.
Contoh Diagram Fasa Larutan Air-Garam
Salah satu contoh diagram fasa yang umum digunakan adalah diagram fasa larutan air-garam.
- Sumbu x menunjukkan konsentrasi garam dalam larutan.
- Sumbu y menunjukkan suhu larutan.
Diagram fasa larutan air-garam dibagi menjadi beberapa daerah:
- Daerah padat (padat)
- Daerah cair (cair)
- Daerah gas (gas)
Titik di mana ketiga daerah bertemu disebut titik tripel, di mana ketiga fase dapat hidup berdampingan dalam kesetimbangan.
Cara Membaca Diagram Fasa
Untuk membaca diagram fasa, carilah titik yang mewakili kondisi sistem yang sedang dipertimbangkan.
Fase sistem ditentukan oleh daerah tempat titik tersebut berada.
Misalnya, jika titik berada di daerah cair, maka sistem berada dalam fase cair.
Jika titik berada pada garis batas antara dua daerah, maka sistem berada dalam kesetimbangan antara dua fase tersebut.
Penurunan Titik Beku
Penurunan titik beku adalah penurunan suhu pembekuan pelarut ketika zat terlarut ditambahkan. Penurunan ini disebabkan oleh pengurangan jumlah molekul pelarut yang bebas untuk membeku, sehingga membutuhkan suhu yang lebih rendah untuk memulai proses pembekuan.
Rumus Penurunan Titik Beku
Rumus penurunan titik beku dinyatakan sebagai berikut:
∆Tb = Kf x m
di mana:
- ∆Tb adalah penurunan titik beku
- Kf adalah konstanta penurunan titik beku pelarut
- m adalah molalitas larutan (mol zat terlarut per kg pelarut)
Tabel Hubungan Konsentrasi dan Penurunan Titik Beku
Tabel berikut menunjukkan hubungan antara konsentrasi zat terlarut dan penurunan titik beku dalam air (Kf = 1,86 °C/m):
| Konsentrasi (m) | Penurunan Titik Beku (°C) |
|---|---|
| 0,1 | 0,186 |
| 0,2 | 0,372 |
| 0,3 | 0,558 |
| 0,4 | 0,744 |
| 0,5 | 0,930 |
Kenaikan Titik Didih
Kenaikan titik didih adalah salah satu sifat koligatif yang terjadi ketika zat terlarut ditambahkan ke dalam pelarut murni, menyebabkan peningkatan titik didih larutan dibandingkan dengan pelarut murni.
Persamaan kenaikan titik didih dirumuskan sebagai berikut:
ΔTb = Kb x m
di mana:
- ΔTb adalah kenaikan titik didih (dalam derajat Celcius)
- Kb adalah konstanta kenaikan titik didih (dalam derajat Celcius/molal)
- m adalah molalitas larutan (dalam mol/kg pelarut)
Hubungan antara konsentrasi zat terlarut dan kenaikan titik didih ditunjukkan dalam diagram berikut:
[Diagram yang menunjukkan hubungan antara konsentrasi zat terlarut dan kenaikan titik didih]
Tekanan Osmotik
Tekanan osmotik adalah gaya yang bekerja pada membran semipermeabel yang memisahkan dua larutan dengan konsentrasi berbeda. Membran semipermeabel hanya memungkinkan pelarut, seperti air, untuk melewatinya, sementara menghalangi zat terlarut.
Rumus Tekanan Osmotik
Tekanan osmotik dapat dihitung menggunakan rumus berikut:
π = MRT
di mana:
- π adalah tekanan osmotik (pascal)
- M adalah konsentrasi molar zat terlarut (mol/L)
- R adalah konstanta gas (8,314 J/mol K)
- T adalah suhu dalam Kelvin
Aplikasi Sifat Koligatif
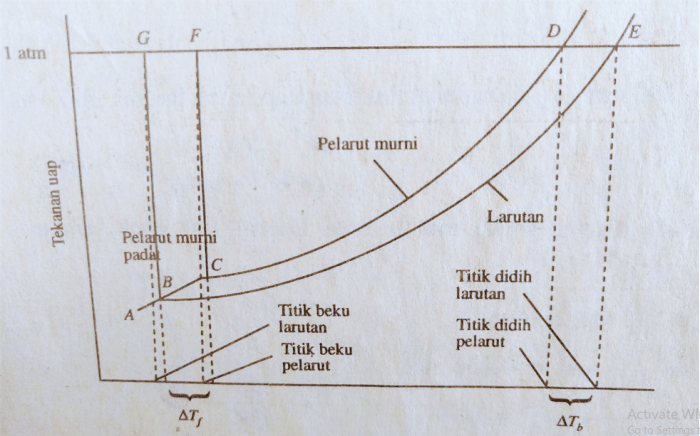
Sifat koligatif memiliki banyak aplikasi dalam kehidupan sehari-hari dan industri.
Contoh Penerapan dalam Kehidupan Sehari-hari
*
-*Pembuatan es krim
Menambahkan garam ke dalam air akan menurunkan titik bekunya, sehingga memperlambat pembentukan kristal es. Ini menghasilkan es krim yang lebih lembut dan halus.
-
-*Pencairan es di jalan
Garam ditaburkan di jalan yang tertutup es untuk menurunkan titik bekunya, mempercepat pencairan es.
-*Memasak
Menambahkan garam ke dalam air mendidih akan meningkatkan titik didihnya, sehingga memungkinkan makanan dimasak pada suhu yang lebih tinggi.
Peran dalam Industri
*
-*Industri makanan
Sifat koligatif digunakan untuk mengontrol kualitas makanan. Misalnya, titik beku susu dapat digunakan untuk mendeteksi pengenceran dengan air.
-
-*Industri farmasi
Sifat koligatif digunakan dalam pengembangan obat. Misalnya, titik beku darah dapat digunakan untuk mendeteksi dehidrasi.
-*Industri otomotif
Sifat koligatif digunakan dalam pengembangan antibeku. Antibeku adalah cairan yang ditambahkan ke radiator mobil untuk menurunkan titik bekunya, mencegah kerusakan mesin pada suhu dingin.
Terakhir

Diagram fasa sifat koligatif memberikan kerangka kerja yang kuat untuk memahami dan memprediksi perilaku larutan.
Dengan bantuan alat grafis ini, kita dapat mengoptimalkan proses kimia, mengembangkan bahan baru, dan memperoleh pemahaman yang lebih komprehensif tentang sistem berbasis larutan yang kompleks. Studi tentang sifat koligatif dan diagram fasa tetap menjadi bidang penelitian aktif, membuka jalan bagi penemuan dan aplikasi baru yang akan terus membentuk pemahaman kita tentang kimia larutan.
Pertanyaan Umum yang Sering Muncul
Apa itu sifat koligatif?
Sifat koligatif adalah sifat larutan yang bergantung pada konsentrasi partikel terlarut, bukan identitas kimianya.
Apa saja jenis-jenis sifat koligatif?
Sifat koligatif meliputi penurunan titik beku, kenaikan titik didih, tekanan osmotik, dan penurunan tekanan uap.
Bagaimana cara membaca diagram fasa larutan air-garam?
Diagram fasa larutan air-garam menunjukkan daerah padat, cair, dan gas pada suhu dan konsentrasi yang berbeda. Garis pada diagram menunjukkan kesetimbangan antara fase-fase ini.