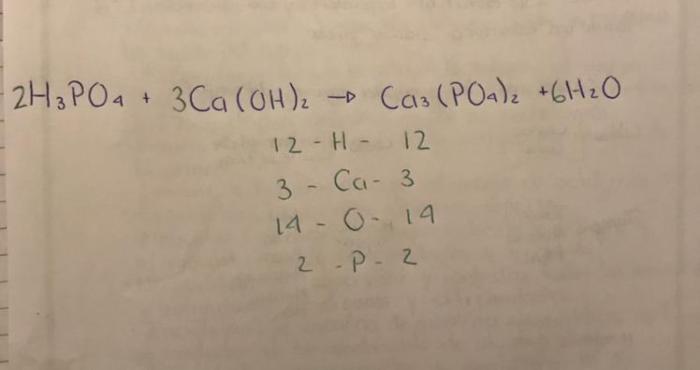Dalam dunia kimia, interaksi antara senyawa anorganik sangat penting untuk dipahami. Salah satu interaksi yang menarik adalah antara kalsium hidroksida (Ca(OH)2), asam fosfat (H3PO4), kalsium fosfat (Ca3(PO4)2), dan air (H2O). Interaksi ini memiliki implikasi penting dalam berbagai bidang, mulai dari biologi hingga material science.
Senyawa-senyawa ini memainkan peran penting dalam proses biologis, seperti pembentukan tulang dan regulasi pH. Selain itu, mereka memiliki aplikasi luas dalam industri, seperti produksi pupuk, bahan bangunan, dan pembersih.
Komposisi Kimia
Komposisi kimia dari Ca(OH)2, H3PO4, Ca3(PO4)2, dan H2O adalah sebagai berikut:
Rumus Kimia, Massa Molar, dan Kelarutan dalam Air
- Ca(OH)2: Kalsium hidroksida, massa molar 74,09 g/mol, larut dalam air
- H3PO4: Asam fosfat, massa molar 97,99 g/mol, larut dalam air
- Ca3(PO4)2: Kalsium fosfat, massa molar 310,18 g/mol, tidak larut dalam air
- H2O: Air, massa molar 18,02 g/mol, larut dalam air
Reaksi Kimia
Ketika kalsium hidroksida (Ca(OH)2) dan asam fosfat (H3PO4) dicampurkan, terjadi reaksi kimia yang menghasilkan kalsium fosfat (Ca3(PO4)2) dan air (H2O).
Persamaan Reaksi Kimia Seimbang
Persamaan reaksi kimia seimbang untuk reaksi ini adalah:
Ca(OH)2 + 2H3PO4 → Ca3(PO4)2 + 6H2O
Contoh Reaksi
Dalam bentuk blok kutipan:
Jika 100 mL larutan Ca(OH)2 0,1 M dicampurkan dengan 100 mL larutan H3PO4 0,1 M, reaksi yang terjadi akan menghasilkan 0,0167 mol Ca3(PO4)2 dan 0,2 mol H2O.
Sifat Fisika
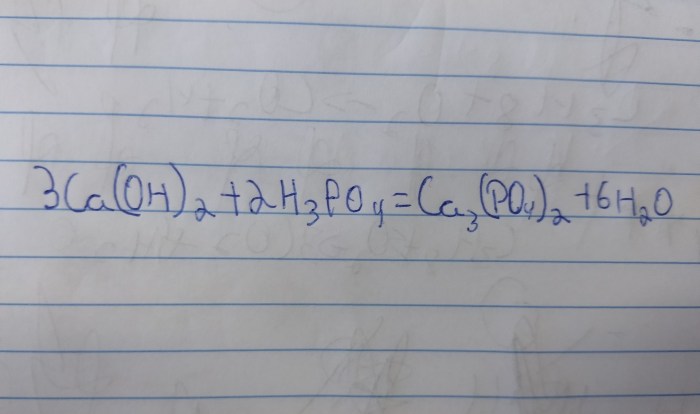
Sifat fisik dari Ca(OH)2, H3PO4, Ca3(PO4)2, dan H2O sangat bervariasi. Beberapa sifat penting yang membedakan senyawa ini meliputi warna, titik leleh, titik didih, dan densitas.
Warna
- Ca(OH)2: Putih
- H3PO4: Tidak berwarna
- Ca3(PO4)2: Putih
- H2O: Tidak berwarna
Titik Leleh
- Ca(OH)2: 580 °C
- H3PO4: 42,35 °C
- Ca3(PO4)2: 1670 °C
- H2O: 0 °C
Titik Didih
- Ca(OH)2: Tidak menguap
- H3PO4: 213 °C
- Ca3(PO4)2: Tidak menguap
- H2O: 100 °C
Densitas
- Ca(OH)2: 2,21 g/cm³
- H3PO4: 1,71 g/cm³
- Ca3(PO4)2: 3,14 g/cm³
- H2O: 1 g/cm³
Kegunaan
Kalsium hidroksida (Ca(OH)2), asam fosfat (H3PO4), kalsium fosfat (Ca3(PO4)2), dan air (H2O) memiliki berbagai kegunaan penting dalam industri, pertanian, dan kehidupan sehari-hari.
Berikut adalah penjelasan lebih lanjut tentang kegunaan masing-masing bahan kimia:
Kalsium Hidroksida (Ca(OH)2)
- Sebagai bahan baku dalam produksi semen dan mortar.
- Sebagai flokulan dalam pengolahan air dan air limbah.
- Sebagai bahan penjernih dalam produksi gula.
- Sebagai aditif dalam makanan sebagai pengatur pH.
Asam Fosfat (H3PO4)
- Sebagai bahan baku dalam produksi pupuk fosfat.
- Sebagai aditif dalam makanan dan minuman sebagai pengatur keasaman.
- Sebagai bahan pembersih karat dan logam.
- Sebagai bahan dalam produksi obat-obatan dan suplemen.
Kalsium Fosfat (Ca3(PO4)2)
- Sebagai bahan baku dalam produksi pupuk fosfat.
- Sebagai aditif dalam makanan sebagai sumber kalsium.
- Sebagai bahan dalam produksi keramik dan porselen.
- Sebagai bahan dalam produksi pasta gigi dan kosmetik.
Air (H2O)
- Sebagai bahan baku dalam produksi banyak produk, termasuk minuman, makanan, dan bahan kimia.
- Sebagai pelarut universal.
- Sebagai bahan pendingin dalam sistem pendingin.
- Sebagai bahan transportasi dalam sistem irigasi dan pipa ledeng.
Produksi dan Pemurnian

Produksi dan pemurnian kalsium hidroksida (Ca(OH)2), asam fosfat (H3PO4), kalsium fosfat (Ca3(PO4)2), dan air (H2O) melibatkan beberapa proses penting. Artikel ini akan membahas metode yang digunakan dalam produksi dan pemurnian masing-masing senyawa.
Produksi Ca(OH)2
Kalsium hidroksida diproduksi melalui proses yang disebut pemadaman kapur . Kapur (kalsium oksida, CaO) direaksikan dengan air dalam reaksi eksotermik:
CaO + H2O → Ca(OH)2 + panas
Produk yang dihasilkan, yang dikenal sebagai susu kapur, kemudian dimurnikan dengan penyaringan dan pengendapan untuk menghilangkan kotoran.
Pemurnian H3PO4
Asam fosfat dapat diproduksi melalui beberapa metode, termasuk:
- Proses Basah: Fosforit (batu fosfat) direaksikan dengan asam sulfat untuk menghasilkan asam fosfat.
- Proses Termal: Fosforit dipanaskan dengan pasir dan kokas untuk menghasilkan fosfor elemental, yang kemudian dibakar untuk menghasilkan asam fosfat.
Asam fosfat yang dihasilkan dimurnikan melalui ekstraksi pelarut dan kristalisasi untuk menghilangkan kotoran.
Produksi Ca3(PO4)2
Kalsium fosfat diproduksi melalui reaksi antara kalsium hidroksida dan asam fosfat:
3Ca(OH)2 + 2H3PO4 → Ca3(PO4)2 + 6H2O
Produk yang dihasilkan dimurnikan dengan pencucian dan pengeringan untuk menghilangkan kotoran.
Pemurnian H2O
Air dapat dimurnikan melalui berbagai metode, termasuk:
- Penyaringan: Menghapus partikel tersuspensi.
- Klorinasi: Membunuh bakteri.
- Osmosis Balik: Menghilangkan garam dan kotoran lainnya.
Metode pemurnian yang digunakan tergantung pada kualitas air dan tujuan penggunaannya.
Akhir Kata

Memahami interaksi kimia antara Ca(OH)2, H3PO4, Ca3(PO4)2, dan H2O sangat penting untuk kemajuan di berbagai bidang. Penelitian lebih lanjut akan membuka jalan bagi pengembangan aplikasi baru dan pemahaman yang lebih baik tentang proses kimia yang mendasari.
Pertanyaan Umum (FAQ)
Apa rumus kimia kalsium fosfat?
Ca3(PO4)2
Apa kegunaan asam fosfat?
Pupuk, aditif makanan, pembersih
Apa warna kalsium hidroksida?
Putih
Apa titik leleh air?
0 derajat Celcius
Bagaimana kalsium fosfat diproduksi?
Reaksi antara kalsium hidroksida dan asam fosfat