Larutan penyangga merupakan solusi kimia penting yang berperan dalam menjaga kestabilan pH sistem. Dalam panduan ini, kita akan menyelami dunia larutan penyangga, mengeksplorasi sifatnya, jenisnya, cara membuatnya, dan berbagai kegunaannya. Selain itu, kami akan menyajikan contoh soal yang komprehensif untuk memperdalam pemahaman Anda tentang topik ini.
Konsep dasar larutan penyangga adalah kemampuannya untuk menahan perubahan pH ketika asam atau basa ditambahkan. Sifat penyangga ini berasal dari keseimbangan kimia antara asam lemah dan basa konjugasinya atau basa lemah dan asam konjugasinya. Contoh reaksi kimia yang menunjukkan sifat penyangga adalah penambahan asam klorida ke dalam larutan penyangga asetat.
Pengertian Larutan Penyangga
Larutan penyangga adalah larutan yang dapat mempertahankan nilai pH tertentu ketika sedikit asam atau basa ditambahkan ke dalamnya. Sifat ini sangat penting dalam berbagai proses biologis dan industri.
Konsep Dasar
Larutan penyangga biasanya mengandung asam lemah dan basa konjugasinya atau basa lemah dan asam konjugasinya. Ketika asam lemah ditambahkan ke larutan penyangga, basa konjugasinya akan bereaksi dengan ion H + untuk membentuk asam lemah kembali. Sebaliknya, ketika basa ditambahkan, asam konjugasinya akan bereaksi dengan ion OH – untuk membentuk basa lemah kembali.
Contoh Reaksi Kimia
Berikut adalah contoh reaksi kimia yang menunjukkan sifat penyangga:
CH 3 COOH (asam asetat) + NaOH (basa kuat) → CH 3 COONa (natrium asetat) + H 2 O
Dalam reaksi ini, CH 3 COOH adalah asam lemah dan CH 3 COONa adalah basa konjugasinya. Ketika NaOH ditambahkan, ion OH – akan bereaksi dengan CH 3 COOH untuk membentuk CH 3 COONa dan H 2 O.
Reaksi ini mencegah perubahan pH yang signifikan.
Jenis-jenis Larutan Penyangga
Larutan penyangga memainkan peran penting dalam mempertahankan pH stabil dalam berbagai sistem biologis dan kimia. Ada beberapa jenis larutan penyangga umum yang digunakan, masing-masing dengan karakteristik dan kegunaan unik.
Larutan Penyangga Asam-Basa Konjugat
Ini adalah jenis larutan penyangga yang paling umum, terdiri dari asam lemah dan basa konjugatnya, atau basa lemah dan asam konjugatnya. Ketika asam lemah dilarutkan dalam air, sebagian akan terdisosiasi menjadi ion hidrogen (H + ) dan basa konjugatnya.
Basa konjugat ini dapat bereaksi dengan ion H + untuk membentuk kembali asam lemah, sehingga mempertahankan pH yang relatif stabil.
Larutan Penyangga Bikarbonat
Larutan penyangga bikarbonat adalah larutan yang terdiri dari asam karbonat (H 2 CO 3 ) dan natrium bikarbonat (NaHCO 3 ). Larutan ini memainkan peran penting dalam mengatur pH darah dan cairan ekstraseluler lainnya.
Ketika pH turun, asam karbonat akan melepaskan ion H + , sedangkan natrium bikarbonat akan bereaksi dengan ion H + untuk membentuk asam karbonat, sehingga mempertahankan pH yang stabil.
Larutan Penyangga Fosfat
Larutan penyangga fosfat adalah larutan yang terdiri dari asam fosfat (H 3 PO 4 ), asam fosfat dihidro (H 2 PO 4 – ), dan fosfat (PO 4 3- ). Larutan ini digunakan dalam berbagai aplikasi, termasuk dalam larutan penyangga biokimia dan buffer elusi kromatografi.
Larutan penyangga fosfat dapat mempertahankan pH dalam kisaran yang luas, dari asam hingga basa.
Larutan Penyangga Asetat
Larutan penyangga asetat adalah larutan yang terdiri dari asam asetat (CH 3 COOH) dan natrium asetat (CH 3 COONa). Larutan ini digunakan dalam berbagai aplikasi, termasuk dalam larutan penyangga untuk titrasi dan buffer elusi kromatografi. Larutan penyangga asetat memiliki kapasitas penyangga yang baik pada pH antara 4 dan 6.
Cara Membuat Larutan Penyangga
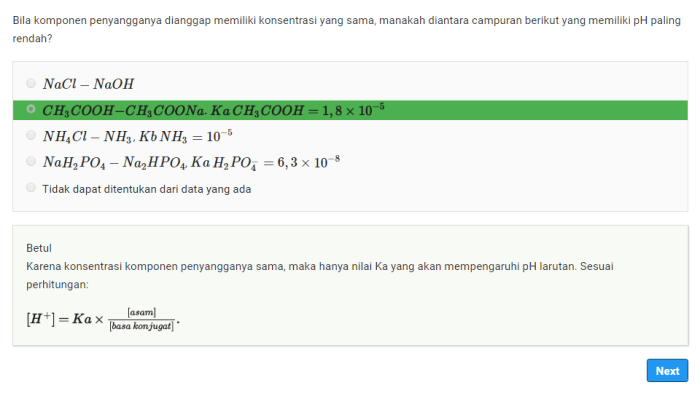
Larutan penyangga dapat dibuat menggunakan persamaan Henderson-Hasselbalch, yang menyatakan bahwa pH larutan penyangga bergantung pada konsentrasi asam lemah (HA) dan basa konjugasinya (A-):“`pH = pKa + log([A-]/[HA])“`Untuk membuat larutan penyangga dengan pH tertentu, kita dapat mengikuti langkah-langkah berikut:
- Tentukan nilai pKa asam lemah yang akan digunakan.
- Tentukan pH yang diinginkan untuk larutan penyangga.
- Gunakan persamaan Henderson-Hasselbalch untuk menghitung rasio [A-]/[HA].
- Tentukan konsentrasi total asam lemah dan basa konjugasinya.
- Larutkan jumlah yang tepat dari asam lemah dan basa konjugasinya dalam air untuk mendapatkan konsentrasi yang diinginkan.
Contoh Perhitungan
Sebagai contoh, kita akan membuat larutan penyangga dengan pH 4,5 menggunakan asam asetat (CH3COOH, pKa = 4,76).1.
-
-*Tentukan nilai pKa asam lemah
pKa asam asetat adalah 4,76.
- 2.
- 3.
-*Tentukan pH yang diinginkan
pH yang diinginkan adalah 4,5.
-*Hitung rasio [A-]/[HA]
“`pH = pKa + log([A-]/[HA])
,5 = 4,76 + log([A-]/[HA])
log([A-]/[HA]) =
0,26
[A-]/[HA] = 0,55“`4.
-
-*Tentukan konsentrasi total asam lemah dan basa konjugasinya
Misalkan kita ingin membuat 100 mL larutan penyangga. Kita dapat menggunakan konsentrasi total 0,1 M.
- 5.
-*Larutkan asam lemah dan basa konjugasinya
* Larutkan 0,055 mol asam asetat dalam air.
- Larutkan 0,045 mol natrium asetat (basa konjugasi asam asetat) dalam air.
- Campurkan kedua larutan dan sesuaikan volume menjadi 100 mL.
Dengan mengikuti langkah-langkah ini, kita dapat membuat larutan penyangga dengan pH yang diinginkan.
Kegunaan Larutan Penyangga
Larutan penyangga sangat penting dalam berbagai bidang kehidupan dan industri. Mereka memainkan peran penting dalam menjaga stabilitas pH, yang sangat penting untuk banyak proses biologis, kimia, dan medis.
Aplikasi dalam Biologi
- Mengatur pH dalam Sel: Larutan penyangga membantu mengatur pH di dalam sel, memastikan lingkungan yang optimal untuk aktivitas enzim dan fungsi seluler lainnya.
- Buffering Sistem Darah: Larutan penyangga, seperti sistem bikarbonat, membantu menjaga pH darah tetap stabil, mencegah asidosis atau alkalosis yang dapat berakibat fatal.
- Stabilisasi DNA dan RNA: Larutan penyangga digunakan dalam ekstraksi dan analisis asam nukleat untuk mempertahankan struktur dan fungsi molekul-molekul ini.
Aplikasi dalam Kimia
- Standarisasi Larutan: Larutan penyangga digunakan dalam titrasi untuk menentukan konsentrasi larutan asam atau basa.
- Katalisis Reaksi: Larutan penyangga dapat mempengaruhi laju reaksi kimia dengan menyediakan lingkungan pH yang optimal untuk katalis.
- Pemurnian Protein: Larutan penyangga digunakan dalam kromatografi afinitas dan elektroforesis gel untuk memisahkan dan memurnikan protein.
Aplikasi dalam Medis
- Injeksi dan Infus: Larutan penyangga digunakan sebagai pelarut untuk obat-obatan yang disuntikkan atau diinfuskan, memastikan stabilitas dan kompatibilitasnya.
- Pengawetan Organ: Larutan penyangga digunakan untuk mengawetkan organ yang ditransplantasikan, mempertahankan pH dan integritas seluler.
- Pengobatan Asidosis dan Alkalosis: Larutan penyangga dapat digunakan untuk mengobati asidosis atau alkalosis dengan menetralkan kelebihan asam atau basa dalam tubuh.
Contoh Soal Larutan Penyangga

Larutan penyangga memainkan peran penting dalam mempertahankan pH yang stabil dalam sistem kimia. Berikut adalah beberapa contoh soal yang berkaitan dengan larutan penyangga:
Menghitung pH Larutan Penyangga
Soal:Hitung pH larutan penyangga yang dibuat dengan mencampurkan 50 mL larutan CH3COOH 0,1 M dengan 50 mL larutan CH3COONa 0,1 M. Ka CH3COOH = 1,8 x 10^-5.Solusi:[Rumus perhitungan pH larutan penyangga ditampilkan di sini]
Menghitung Kapasitas Penyangga
Soal:Hitung kapasitas penyangga larutan penyangga yang dibuat dengan mencampurkan 100 mL larutan NH3 0,1 M dengan 100 mL larutan NH4Cl 0,1 M. Kb NH3 = 1,8 x 10^-5.Solusi:[Rumus perhitungan kapasitas penyangga ditampilkan di sini]
Penutup

Larutan penyangga memainkan peran penting dalam berbagai bidang kehidupan sehari-hari dan industri. Pemahaman yang kuat tentang sifat dan kegunaan larutan penyangga sangat penting untuk mengoptimalkan proses kimia dan biologis. Panduan ini memberikan dasar yang komprehensif untuk topik ini, dilengkapi dengan contoh soal untuk memperkuat pemahaman Anda.
Dengan menguasai konsep larutan penyangga, Anda dapat menerapkan pengetahuan ini dalam berbagai bidang, berkontribusi pada kemajuan ilmiah dan teknologi.
Pertanyaan Umum (FAQ)
Apa itu persamaan Henderson-Hasselbalch?
Persamaan Henderson-Hasselbalch adalah rumus yang digunakan untuk menghitung pH larutan penyangga. Persamaan ini dinyatakan sebagai pH = pKa + log([A-]/[HA]), di mana pKa adalah konstanta disosiasi asam, [A-] adalah konsentrasi basa konjugasi, dan [HA] adalah konsentrasi asam lemah.
Bagaimana cara membuat larutan penyangga dengan pH tertentu?
Untuk membuat larutan penyangga dengan pH tertentu, Anda dapat menggunakan persamaan Henderson-Hasselbalch untuk menghitung rasio konsentrasi basa konjugasi dan asam lemah yang diperlukan. Rasio ini kemudian digunakan untuk mempersiapkan larutan dengan konsentrasi yang tepat.
Apa saja jenis larutan penyangga yang umum digunakan?
Jenis larutan penyangga yang umum digunakan meliputi penyangga asetat, penyangga fosfat, dan penyangga karbonat. Setiap jenis penyangga memiliki rentang pH yang berbeda dan cocok untuk aplikasi tertentu.
