Hidrokarbon, senyawa organik yang hanya terdiri dari atom karbon dan hidrogen, merupakan pilar kehidupan modern. Di antara berbagai jenis hidrokarbon, alkana, alkena, alkuna, dan alkil menonjol karena peran pentingnya dalam industri, produk konsumen, dan proses biologis.
Dalam tulisan ini, kita akan mengeksplorasi sifat unik, metode pembuatan, kegunaan, dan hubungan antara alkana, alkena, alkuna, dan alkil. Pengetahuan ini sangat penting untuk memahami kimia organik dan aplikasinya yang luas.
Pengertian Alkana, Alkena, dan Alkuna
Alkana, alkena, dan alkuna adalah tiga jenis hidrokarbon, senyawa yang hanya mengandung atom karbon dan hidrogen. Ketiganya memiliki sifat kimia yang berbeda berdasarkan struktur molekulnya.
Alkana
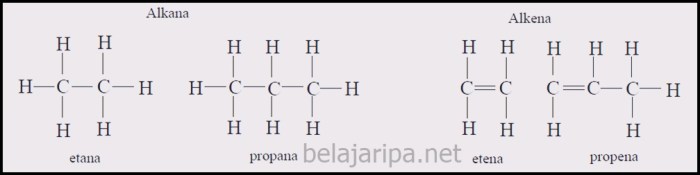
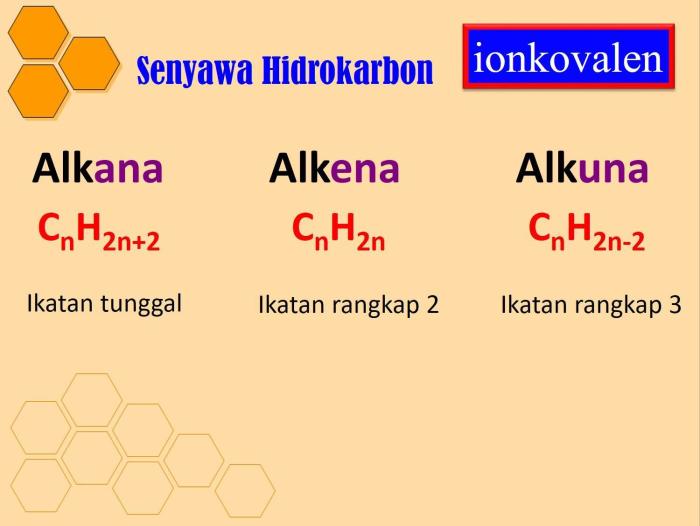
Alkana adalah hidrokarbon jenuh, yang berarti semua atom karbonnya terikat satu sama lain dengan ikatan tunggal. Mereka memiliki rumus umum CnH2n+2, di mana n adalah jumlah atom karbon dalam molekul. Metana (CH4), etana (C2H6), dan propana (C3H8) adalah contoh alkana.
Alkena
Alkena adalah hidrokarbon tak jenuh yang memiliki setidaknya satu ikatan rangkap dua antara dua atom karbon. Rumus umum alkena adalah CnH2n. Etena (C2H4), propen (C3H6), dan butena (C4H8) adalah contoh alkena.
Alkuna
Alkuna adalah hidrokarbon tak jenuh yang memiliki setidaknya satu ikatan rangkap tiga antara dua atom karbon. Rumus umum alkuna adalah CnH2n-2. Euna (C2H2), propuna (C3H4), dan butuna (C4H6) adalah contoh alkuna.
Sifat Fisika dan Kimia Alkana, Alkena, dan Alkuna
Alkana, alkena, dan alkuna adalah tiga jenis hidrokarbon yang memiliki sifat fisika dan kimia yang berbeda. Perbedaan ini disebabkan oleh perbedaan dalam struktur dan ikatan kimianya.
Sifat Fisika
| Jenis Hidrokarbon | Titik Leleh (°C) | Titik Didih (°C) | Kerapatan (g/cm³) |
|---|---|---|---|
| Alkana | -183 | -89 | 0,7 |
| Alkena | -169 | -10 | 0,7 |
| Alkuna | -81 | 84 | 0,7 |
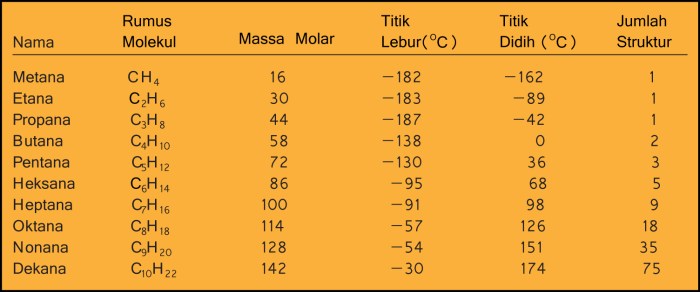
Seperti yang ditunjukkan pada tabel, titik leleh dan titik didih alkana, alkena, dan alkuna meningkat seiring dengan bertambahnya jumlah atom karbon dalam molekul. Hal ini karena semakin banyak atom karbon, semakin kuat gaya van der Waals yang bekerja antar molekul.
Kerapatan alkana, alkena, dan alkuna relatif sama. Ketiganya memiliki kerapatan yang lebih rendah dari air, sehingga akan mengapung di atas air.
Sifat Kimia
Alkana, alkena, dan alkuna memiliki reaktivitas yang berbeda. Alkana adalah yang paling tidak reaktif, sedangkan alkuna adalah yang paling reaktif. Reaktivitas yang berbeda ini disebabkan oleh perbedaan dalam ikatan kimianya.
Alkana memiliki ikatan tunggal antara atom karbon, yang merupakan ikatan yang kuat dan sulit diputus. Alkena memiliki ikatan rangkap antara atom karbon, yang merupakan ikatan yang lebih lemah dan lebih mudah diputus. Alkuna memiliki ikatan rangkap tiga antara atom karbon, yang merupakan ikatan yang paling lemah dan paling mudah diputus.
Karena perbedaan dalam reaktivitasnya, alkana, alkena, dan alkuna dapat bereaksi dengan berbagai macam reagen. Alkana umumnya bereaksi melalui reaksi substitusi, sedangkan alkena dan alkuna dapat bereaksi melalui reaksi adisi dan substitusi.
Cara Pembuatan Alkana, Alkena, dan Alkuna
Pembuatan Alkana
- Reaksi Hidrogenasi Alkena: Mereaksikan alkena dengan gas hidrogen (H2) menggunakan katalis seperti paladium (Pd) atau nikel (Ni) menghasilkan alkana.
- Reaksi Reduksi Alkil Halida: Mereaksikan alkil halida dengan logam seperti natrium (Na) atau litium aluminium hidrida (LiAlH4) menghasilkan alkana.
- Reaksi Wurtz: Mereaksikan dua alkil halida yang sama dengan natrium dalam pelarut eter menghasilkan alkana.
Pembuatan Alkena
- Reaksi Dehidrasi Alkohol: Mereaksikan alkohol dengan asam kuat seperti asam sulfat (H2SO4) atau asam fosfat (H3PO4) menghasilkan alkena.
- Reaksi Eliminasi Alkil Halida: Mereaksikan alkil halida dengan basa kuat seperti kalium hidroksida (KOH) atau natrium etoksida (NaOEt) menghasilkan alkena.
- Reaksi Pemanasan Alkil Halida: Pemanasan alkil halida tertentu seperti 2-bromopropana dengan basa menghasilkan alkena.
Pembuatan Alkuna
- Reaksi Dehidrohalogenasi Dihalida Geminal: Mereaksikan dihalida geminal (dua atom halogen pada atom karbon yang sama) dengan basa kuat menghasilkan alkuna.
- Reaksi Kondensasi Karbonil: Mereaksikan dua molekul karbonil (aldehida atau keton) dengan basa kuat menghasilkan alkuna.
- Reaksi Eliminasi Berbasis Karbon: Pemanasan senyawa tertentu seperti 1,2-dibromoetana dengan logam seperti perak (Ag) atau tembaga (Cu) menghasilkan alkuna.
Kegunaan Alkana, Alkena, dan Alkuna
Alkana, alkena, dan alkuna adalah tiga jenis utama hidrokarbon yang banyak digunakan dalam kehidupan sehari-hari. Masing-masing jenis memiliki sifat dan kegunaan unik dalam berbagai industri dan produk konsumen.
Alkana
- Sebagai bahan bakar, seperti propana (C3H8) dan butana (C4H10)
- Pembuatan lilin, parafin, dan pelumas
- Bahan baku industri petrokimia untuk memproduksi plastik, karet sintetis, dan deterjen
Alkena
- Bahan baku untuk memproduksi plastik, seperti polietilen (C2H4) dan polipropilen (C3H6)
- Pembuatan karet sintetis, seperti polibutadiena (C4H6)
- Sebagai bahan baku industri kimia untuk memproduksi alkohol, aldehida, dan asam karboksilat
Alkuna
- Sebagai bahan baku untuk memproduksi karet sintetis, seperti poliasetilena (C2H2)
- Pembuatan plastik, seperti polivinil asetilena (C4H4)
- Sebagai bahan baku industri kimia untuk memproduksi alkena, aldehida, dan keton
Reaksi Alkilasi

Reaksi alkilasi adalah reaksi kimia yang melibatkan penggantian atom hidrogen pada sebuah molekul dengan gugus alkil. Reaksi ini sangat penting dalam sintesis organik dan digunakan dalam produksi berbagai senyawa, termasuk obat-obatan, bahan bakar, dan plastik.
Contoh Reaksi Alkilasi
Salah satu contoh reaksi alkilasi adalah reaksi antara natrium etoksida dan etil bromida, yang menghasilkan etil eter:
CH 3 CH 2 ONa + CH 3 CH 2 Br → CH 3 CH 2 OCH 2 CH 3 + NaBr
Dalam reaksi ini, gugus etoksida (CH 3 CH 2 O-) menggantikan atom hidrogen pada etil bromida, menghasilkan etil eter. Mekanisme reaksi ini melibatkan serangan nukleofilik gugus etoksida pada atom karbon yang bermuatan positif pada etil bromida.
Identifikasi Alkil
Gugus alkil merupakan gugus hidrokarbon jenuh yang terdiri dari atom karbon dan hidrogen yang terikat dengan ikatan tunggal. Gugus ini merupakan bagian penting dari banyak senyawa organik, termasuk alkana, alkena, dan alkuna.
Cara Mengidentifikasi Gugus Alkil
Untuk mengidentifikasi gugus alkil dalam molekul organik, ikuti langkah-langkah berikut:
- Identifikasi atom karbon yang tidak terikat dengan atom oksigen, nitrogen, atau halogen.
- Hitung jumlah atom karbon dalam gugus yang terhubung dengan atom karbon yang diidentifikasi pada langkah 1.
- Tambahkan akhiran “-il” ke jumlah atom karbon yang dihitung pada langkah 2.
Jenis-jenis Gugus Alkil
Jenis-jenis gugus alkil diklasifikasikan berdasarkan jumlah atom karbon yang dikandungnya:
| Nama Gugus Alkil | Jumlah Atom Karbon | Contoh |
|---|---|---|
| Metil | 1 | -CH3 |
| Etil | 2 | -CH2CH3 |
| Propil | 3 | -CH2CH2CH3 |
| Butil | 4 | -CH2CH2CH2CH3 |
| Pentil | 5 | -CH2CH2CH2CH2CH3 |