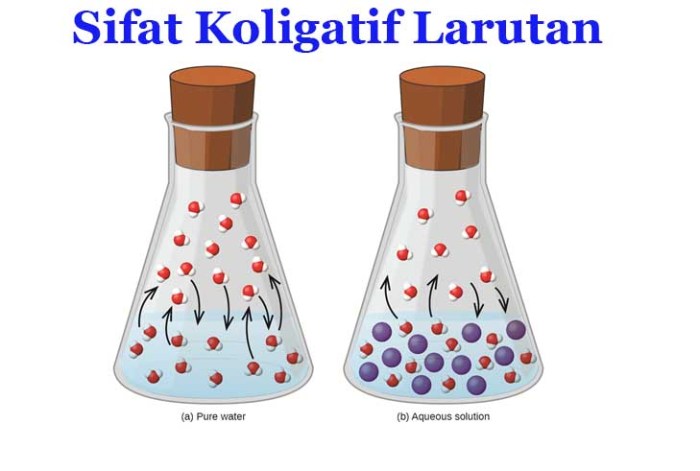
Sifat koligatif adalah sifat-sifat larutan yang bergantung pada jumlah partikel zat terlarut, bukan jenis zat terlarutnya. Sifat-sifat ini memberikan informasi penting tentang konsentrasi dan sifat fisik larutan.
Dalam artikel ini, kita akan membahas konsep sifat koligatif, berbagai jenisnya, dan penerapannya dalam kehidupan sehari-hari dan industri. Kita juga akan memberikan contoh soal dan pembahasan untuk memperkuat pemahaman.
Pengertian Sifat Koligatif
Sifat koligatif adalah sifat larutan yang bergantung pada konsentrasi partikel zat terlarut, bukan pada sifat zat terlarut itu sendiri.
Sifat koligatif penting dalam berbagai bidang, seperti kimia, biologi, dan farmasi. Sifat-sifat ini digunakan untuk menentukan konsentrasi larutan, massa molar zat terlarut, dan sifat-sifat lain dari larutan.
Contoh Sifat Koligatif
- Penurunan tekanan uap
- Kenaikan titik didih
- Penurunan titik beku
- Tekanan osmotik
Jenis-jenis Sifat Koligatif

Sifat koligatif adalah sifat larutan yang bergantung pada konsentrasi partikel terlarut, bukan pada sifat kimia partikel tersebut. Ada empat jenis utama sifat koligatif:
- Penurunan Tekanan Uap
- Kenaikan Titik Didih
- Penurunan Titik Beku
- Tekanan Osmotik
Penerapan Sifat Koligatif

Sifat koligatif merupakan sifat larutan yang hanya bergantung pada konsentrasi partikel terlarut, bukan pada jenis partikelnya. Sifat ini memiliki banyak penerapan dalam kehidupan sehari-hari dan industri.
Contoh Penerapan dalam Kehidupan Sehari-hari
*
-*Membuat es krim
Penambahan garam ke dalam es krim menurunkan titik bekunya, sehingga es krim menjadi lebih lembut dan tidak mudah mengkristal.
-
-*Mencairkan es di jalan
Garam ditaburkan di jalan yang tertutup es untuk menurunkan titik bekunya dan mempercepat pencairan es.
-*Mencegah pembekuan air pada aki mobil
Etilen glikol ditambahkan ke air aki untuk menurunkan titik bekunya dan mencegah air aki membeku pada suhu rendah.
Aplikasi Industri Sifat Koligatif
*
-*Pemisahan isotop
Metode distilasi fraksional memanfaatkan perbedaan titik didih isotop untuk memisahkannya.
-
-*Penentuan massa molekul
Penurunan titik beku atau titik didih larutan dapat digunakan untuk menentukan massa molekul zat terlarut.
-*Pengendalian titik beku
Penambahan antibeku ke radiator mobil menurunkan titik bekunya dan mencegah mesin membeku pada suhu rendah.
-*Penentuan konsentrasi larutan
Titik beku atau titik didih larutan dapat digunakan untuk menentukan konsentrasinya.
-*Desalinasi air laut
Proses osmosis balik menggunakan membran semipermeabel untuk menghilangkan garam dari air laut, menghasilkan air tawar.
Faktor-faktor yang Mempengaruhi Sifat Koligatif

Sifat koligatif larutan dipengaruhi oleh beberapa faktor, antara lain:
- Jumlah partikel zat terlarut
- Sifat pelarut
- Suhu
Jumlah Partikel Zat Terlarut
Semakin banyak partikel zat terlarut yang ditambahkan ke dalam pelarut, semakin besar nilai sifat koligatif larutan. Hal ini disebabkan oleh peningkatan jumlah partikel yang berinteraksi dengan molekul pelarut.
Sifat Pelarut
Sifat pelarut juga mempengaruhi sifat koligatif larutan. Pelarut dengan titik didih yang lebih tinggi memiliki sifat koligatif yang lebih kecil dibandingkan dengan pelarut dengan titik didih yang lebih rendah.
Suhu
Suhu juga mempengaruhi sifat koligatif larutan. Pada suhu yang lebih tinggi, nilai sifat koligatif larutan akan semakin besar. Hal ini disebabkan oleh peningkatan energi kinetik molekul yang menyebabkan lebih banyak partikel yang berinteraksi dengan molekul pelarut.
Contoh Soal dan Pembahasan Sifat Koligatif
Sifat koligatif merupakan sifat larutan yang bergantung pada jumlah partikel zat terlarut, bukan jenis zat terlarutnya. Berikut adalah beberapa contoh soal dan pembahasannya:
Penurunan Titik Beku
Sebuah larutan dibuat dengan melarutkan 10 gram urea (Mr = 60 g/mol) dalam 100 gram air. Hitunglah penurunan titik beku larutan tersebut.Pembahasan:
1. Hitung molalitas larutan
“`Molalitas = (Massa zat terlarut / Mr zat terlarut) / Massa pelarut= (10 g / 60 g/mol) / 100 g= 0,167 mol/kg“`
2. Hitung penurunan titik beku
“`ΔTb = Kf x Molalitas= 1,86 °C/mol/kg x 0,167 mol/kg= 0,31 °C“`Jadi, penurunan titik beku larutan adalah 0,31 °C.
Kenaikan Titik Didih
Sebuah larutan sukrosa (Mr = 342 g/mol) dibuat dengan konsentrasi 0,5 M. Hitunglah kenaikan titik didih larutan tersebut.Pembahasan:
1. Hitung molalitas larutan
“`Molalitas = Konsentrasi x Mr zat terlarut= 0,5 M x 342 g/mol= 171 mol/kg“`
2. Hitung kenaikan titik didih
“`ΔTd = Kb x Molalitas= 0,512 °C/mol/kg x 171 mol/kg= 87,4 °C“`Jadi, kenaikan titik didih larutan adalah 87,4 °C.
Ringkasan Penutup
Pemahaman tentang sifat koligatif sangat penting dalam berbagai bidang kimia. Sifat-sifat ini membantu kita menentukan konsentrasi larutan, memprediksi titik beku dan titik didih larutan, serta memahami proses penting seperti osmosis dan tekanan osmotik. Dengan menguasai sifat koligatif, kita dapat memperoleh wawasan yang lebih dalam tentang perilaku larutan dan aplikasi praktisnya.
Ringkasan FAQ
Apa saja contoh soal sifat koligatif?
Contoh soal sifat koligatif meliputi: menentukan penurunan titik beku larutan, kenaikan titik didih larutan, tekanan osmotik, dan massa molar zat terlarut.
Bagaimana cara menghitung penurunan titik beku larutan?
Penurunan titik beku larutan dapat dihitung menggunakan persamaan ΔTb = Kf x m, di mana ΔTb adalah penurunan titik beku, Kf adalah konstanta penurunan titik beku pelarut, dan m adalah molalitas larutan.
Apa saja aplikasi sifat koligatif dalam kehidupan sehari-hari?
Sifat koligatif digunakan dalam berbagai aplikasi sehari-hari, seperti pembuatan antibeku, cairan pendingin, dan garam pencair es.