Dalam kimia, ikatan kovalen koordinasi memainkan peran penting dalam menentukan sifat dan reaktivitas senyawa. Salah satu senyawa yang menarik yang menampilkan ikatan ini adalah asam sulfat (H2SO4). Artikel ini akan mengeksplorasi konsep ikatan kovalen koordinasi dalam H2SO4, sifat-sifatnya yang unik, aplikasi industri, dan prosedur sintesis senyawa yang melibatkan ikatan ini.
Ikatan kovalen koordinasi, juga dikenal sebagai ikatan datif, terjadi ketika pasangan elektron bebas disumbangkan oleh satu atom atau ion (donor) ke orbital kosong dari atom atau ion lain (akseptor). Dalam H2SO4, ikatan kovalen koordinasi terbentuk antara atom sulfur pusat dan molekul atau ion lain yang memiliki pasangan elektron bebas, seperti air atau amonia.
Ikatan Kovalen Koordinasi H2SO4

Ikatan kovalen koordinasi adalah jenis ikatan kovalen di mana kedua elektron ikatan berasal dari satu atom.
Konsep Ikatan Kovalen Koordinasi
Dalam ikatan kovalen koordinasi, atom donor menyumbangkan sepasang elektron bebas ke atom penerima, yang memiliki orbital kosong. Pasangan elektron ini membentuk ikatan kovalen, dan kedua atom berbagi elektron.
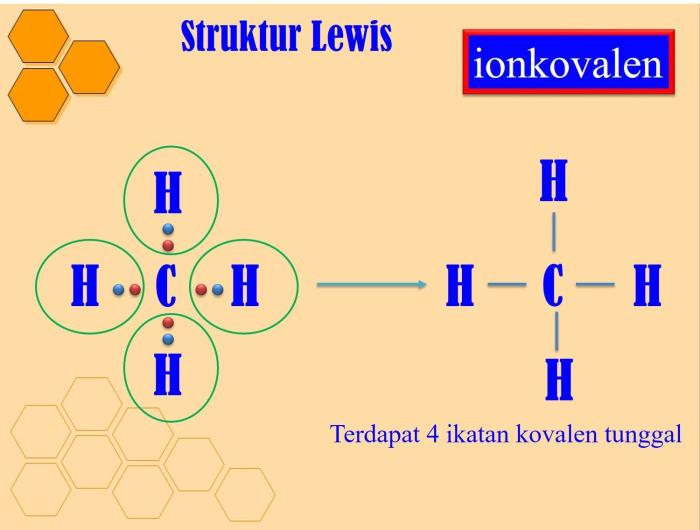
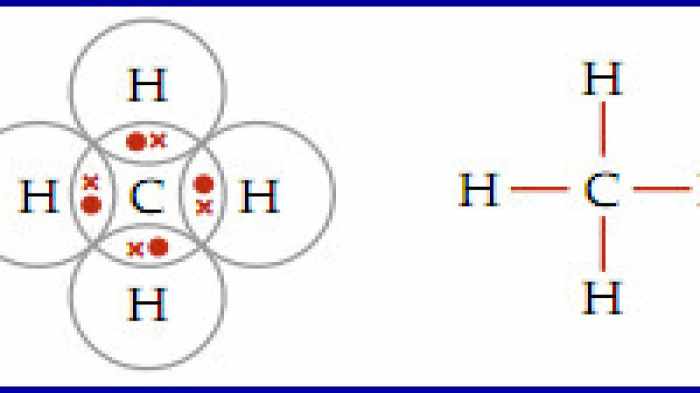
Struktur Lewis H2SO4
Struktur Lewis H2SO4 menunjukkan adanya dua ikatan O-H tunggal dan dua ikatan O=S ganda. Atom sulfur pusat memiliki dua pasangan elektron bebas.
Ikatan Koordinasi dalam H2SO4
Pasangan elektron bebas pada atom sulfur dapat berikatan secara koordinasi dengan ion logam, seperti Fe 3+ , membentuk ikatan Fe-O. Ikatan koordinasi ini memperkuat ikatan antara ion logam dan ligan (H2SO4).
Sifat Ikatan Kovalen Koordinasi H2SO4
Ikatan kovalen koordinasi dalam H2SO4 melibatkan transfer sepasang elektron dari atom donor (belerang) ke atom penerima (oksigen). Ikatan ini mempengaruhi kekuatan, polaritas, stabilitas, dan reaktivitas molekul H2SO4.
Kekuatan dan Polaritas Ikatan
Ikatan kovalen koordinasi dalam H2SO4 relatif kuat karena adanya pasangan elektron terbagi. Polaritas ikatan ini dipengaruhi oleh perbedaan keelektronegatifan antara belerang dan oksigen, dengan belerang yang lebih elektronegatif. Hal ini menghasilkan pembagian elektron yang tidak merata, sehingga atom oksigen sedikit bermuatan negatif dan atom belerang sedikit bermuatan positif.
Stabilitas dan Reaktivitas
Ikatan koordinasi memberikan stabilitas pada molekul H2SO4. Pasangan elektron terbagi mengurangi muatan formal pada atom belerang, sehingga menurunkan energi molekul. Ikatan ini juga meningkatkan reaktivitas H2SO4 karena atom oksigen yang bermuatan negatif menjadi lebih rentan terhadap serangan nukleofilik.
Perbandingan dengan Jenis Ikatan Lainnya
Ikatan kovalen koordinasi dalam H2SO4 berbeda dari jenis ikatan kimia lainnya. Dibandingkan dengan ikatan kovalen normal, ikatan koordinasi memiliki kekuatan yang lebih besar karena adanya transfer elektron penuh. Dibandingkan dengan ikatan ionik, ikatan koordinasi memiliki sifat yang lebih kovalen karena adanya pasangan elektron terbagi.
Perbedaan ini mempengaruhi sifat fisik dan kimia molekul yang terlibat.
Prosedur Sintesis Senyawa dengan Ikatan Kovalen Koordinasi H2SO4

Sintesis senyawa dengan ikatan kovalen koordinasi H2SO4 melibatkan reaksi antara asam sulfat (H2SO4) dan basa Lewis. Berikut adalah prosedur umum yang digunakan:
Bahan
- Asam sulfat (H2SO4)
- Basa Lewis (misalnya, NH3, H2O)
- Pelarut inert (misalnya, air, etanol)
Prosedur
- Larutkan asam sulfat dalam pelarut inert.
- Tambahkan basa Lewis ke dalam larutan asam sulfat secara perlahan, sambil mengaduk terus.
- Reaksikan campuran pada suhu dan waktu yang sesuai.
- Pisahkan senyawa produk dari larutan reaksi menggunakan metode yang sesuai (misalnya, filtrasi, kristalisasi).
Ilustrasi Langkah demi Langkah
- Tambahkan H2SO4 ke dalam pelarut inert (misalnya, air) dan aduk hingga larut.
- Tambahkan basa Lewis (misalnya, NH3) ke dalam larutan H2SO4 secara perlahan, sambil mengaduk terus.
- Amati pembentukan endapan atau perubahan warna, yang menunjukkan pembentukan kompleks koordinasi.
- Panaskan campuran pada suhu yang sesuai (misalnya, 50-80 °C) selama waktu yang ditentukan.
- Biarkan campuran dingin dan pisahkan senyawa produk dari larutan menggunakan filtrasi atau kristalisasi.
Faktor yang Mempengaruhi Hasil Sintesis
Hasil sintesis dipengaruhi oleh beberapa faktor, antara lain:
- Konsentrasi reaktan
- Stoikiometri reaksi
- Suhu dan waktu reaksi
- Jenis pelarut
Untuk mengoptimalkan hasil sintesis, faktor-faktor ini perlu dioptimalkan. Misalnya, konsentrasi reaktan dan suhu reaksi dapat disesuaikan untuk meningkatkan hasil produk.
Simpulan Akhir

Ikatan kovalen koordinasi dalam H2SO4 memiliki implikasi yang signifikan dalam kimia industri, pengolahan air, dan pengolahan limbah. Memahami sifat dan aplikasi ikatan ini sangat penting untuk mengembangkan proses kimia baru, mengoptimalkan reaksi katalitik, dan mengatasi tantangan lingkungan.
Pertanyaan Umum yang Sering Muncul
Apa perbedaan antara ikatan kovalen koordinasi dan ikatan kovalen normal?
Dalam ikatan kovalen normal, kedua atom berkontribusi sama terhadap pasangan elektron yang dibagi, sedangkan dalam ikatan kovalen koordinasi, satu atom menyumbangkan kedua elektron.
Apa aplikasi industri penting dari H2SO4 yang melibatkan ikatan kovalen koordinasi?
H2SO4 digunakan sebagai katalis dalam produksi asam asetat, rayon, dan berbagai bahan kimia lainnya.