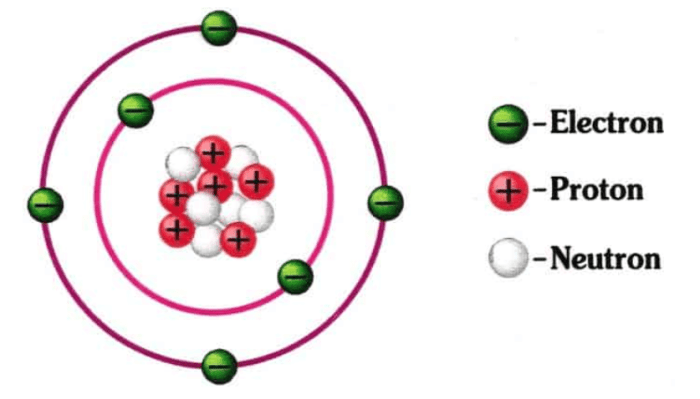
Dalam dunia kimia, atom-atom yang memiliki sifat serupa namun berbeda dalam hal jumlah partikel subatomiknya merupakan topik yang menarik. Isotop, isobar, dan isoton adalah istilah yang menggambarkan atom-atom tersebut, memberikan wawasan tentang kompleksitas dan keragaman alam atom.
Setiap istilah mewakili jenis atom tertentu dengan karakteristik uniknya. Isotop, isobar, dan isoton memiliki aplikasi luas dalam berbagai bidang, mulai dari kedokteran hingga industri, menyoroti pentingnya memahami sifat-sifatnya.
Isotop

Isotop adalah varian suatu unsur kimia yang memiliki jumlah proton yang sama tetapi berbeda jumlah neutronnya. Perbedaan jumlah neutron menyebabkan perbedaan massa atom, namun tidak mengubah sifat kimia dasar unsur tersebut.
Setiap unsur dapat memiliki beberapa isotop yang disebut nuklida. Nuklida dilambangkan dengan simbol unsur, diikuti dengan tanda hubung dan nomor massa (jumlah proton dan neutron dalam nukleus). Misalnya, karbon-12 ( 12 C) memiliki 6 proton dan 6 neutron, sedangkan karbon-14 ( 14 C) memiliki 6 proton dan 8 neutron.
Sifat Isotop
- Memiliki sifat kimia yang sama dengan unsur aslinya.
- Memiliki massa atom yang berbeda karena perbedaan jumlah neutron.
- Dapat dibedakan berdasarkan sifat fisik, seperti massa, waktu paruh (untuk isotop radioaktif), dan sifat spektroskopi.
Contoh Isotop
- Hidrogen: 1H (protium), 2H (deuterium), 3H (tritium)
- Karbon: 12C, 13C, 14C
- Uranium: 235U, 238U
Isobar
Isobar adalah atom-atom dari unsur yang berbeda yang memiliki nomor massa yang sama. Dengan kata lain, isobar memiliki jumlah proton dan neutron yang sama, tetapi jumlah elektronnya berbeda. Isobar dapat terbentuk melalui proses peluruhan radioaktif, di mana inti atom kehilangan atau memperoleh neutron.
Sifat-Sifat Isobar
* Memiliki nomor massa yang sama
- Memiliki jumlah proton dan neutron yang sama
- Memiliki jumlah elektron yang berbeda
- Mempunyai sifat kimia yang mirip, karena memiliki jumlah elektron valensi yang sama
Tabel Perbandingan Isotop dan Isobar
| Karakteristik | Isotop | Isobar ||—|—|—|| Nomor atom | Sama | Berbeda || Nomor massa | Sama | Sama || Jumlah proton | Sama | Berbeda || Jumlah neutron | Berbeda | Sama || Jumlah elektron | Sama | Berbeda || Sifat kimia | Berbeda | Mirip |
Contoh Isobar
Salah satu contoh isobar adalah kalium-40 ( 40 K) dan kalsium-40 ( 40 Ca). Kedua atom ini memiliki nomor massa 40, tetapi kalium memiliki 19 proton dan 21 neutron, sedangkan kalsium memiliki 20 proton dan 20 neutron.
Kedua atom ini memiliki sifat kimia yang mirip karena memiliki jumlah elektron valensi yang sama, yaitu 2.Contoh lain dari isobar adalah karbon-14 ( 14 C) dan nitrogen-14 ( 14 N). Kedua atom ini memiliki nomor massa 14, tetapi karbon memiliki 6 proton dan 8 neutron, sedangkan nitrogen memiliki 7 proton dan 7 neutron.
Kedua atom ini memiliki sifat kimia yang berbeda karena memiliki jumlah elektron valensi yang berbeda, yaitu 4 untuk karbon dan 5 untuk nitrogen.
Isoton
Isoton adalah nuklida yang memiliki jumlah neutron yang sama, tetapi jumlah proton dan elektron yang berbeda. Ini berarti mereka memiliki nomor massa yang sama, tetapi nomor atom yang berbeda.
Sifat-sifat isoton meliputi:
- Memiliki nomor massa yang sama (A)
- Memiliki jumlah neutron yang sama (N)
- Memiliki jumlah proton (Z) dan elektron yang berbeda
- Terletak pada garis miring isobarik pada tabel periodik
Perbedaan Isoton dan Isotop
Isoton berbeda dari isotop, yang memiliki jumlah proton yang sama tetapi jumlah neutron yang berbeda. Akibatnya, isoton memiliki sifat kimia yang berbeda, sedangkan isotop memiliki sifat kimia yang sama.
Contoh Isoton
Contoh isoton adalah:
- 12C, 13N, dan 14O (semua memiliki 7 neutron)
- 35Cl, 36Ar, dan 37K (semua memiliki 20 neutron)
Isoton memiliki aplikasi penting dalam berbagai bidang, seperti penanggalan radioaktif dan pencitraan medis.
Aplikasi Isotop, Isobar, dan Isoton
Isotop, isobar, dan isoton memiliki aplikasi luas dalam berbagai bidang, termasuk kedokteran, industri, dan penelitian. Masing-masing jenis nuklida ini memiliki kegunaan spesifik karena sifat uniknya.
Aplikasi Isotop
- Medis: Isotop radioaktif seperti yodium-131 digunakan dalam pencitraan dan pengobatan penyakit tiroid. Isotop karbon-14 digunakan dalam penanggalan radiokarbon.
- Industri: Isotop stabil seperti deuterium digunakan sebagai moderator dalam reaktor nuklir. Isotop kobalt-60 digunakan dalam radiografi industri.
- Penelitian: Isotop digunakan sebagai pelacak dalam eksperimen ilmiah untuk mempelajari proses biologis dan kimia.
Aplikasi Isobar
- Medis: Isobar radioaktif seperti teknesium-99m digunakan dalam pencitraan medis. Isobar kobalt-57 digunakan dalam pengobatan kanker.
- Industri: Isobar digunakan dalam pengukur kepadatan dan pelacak dalam proses industri.
- Penelitian: Isobar digunakan dalam studi fisika nuklir untuk menyelidiki sifat inti atom.
Aplikasi Isoton
- Medis: Isoton radioaktif seperti natrium-22 digunakan dalam pencitraan jantung. Isoton kalium-40 digunakan dalam penanggalan kalium-argon.
- Industri: Isoton digunakan dalam pembuatan baterai nuklir dan sebagai sumber energi untuk pesawat ruang angkasa.
- Penelitian: Isoton digunakan dalam studi astrofisika untuk menentukan komposisi bintang dan galaksi.
Tren dan Perkembangan

Penelitian dan aplikasi isotop, isobar, dan isoton terus berkembang, membuka jalan bagi terobosan baru dan pemahaman yang lebih mendalam tentang dunia fisik.
Salah satu tren penting adalah penggunaan isotop stabil sebagai pelacak dalam studi lingkungan dan medis. Dengan mengukur rasio isotop yang berbeda, para ilmuwan dapat melacak pergerakan polutan, memahami siklus biogeokimia, dan mendiagnosis penyakit.
Aplikasi Medis
- Pemindaian PET (Positron Emission Tomography) menggunakan isotop radioaktif untuk mendeteksi dan memantau penyakit.
- Terapi radiasi menggunakan isotop radioaktif untuk menargetkan dan menghancurkan sel kanker.
- Studi metabolomik menggunakan isotop stabil untuk mengidentifikasi dan mengukur metabolit dalam tubuh, membantu mendiagnosis dan memantau penyakit.
Aplikasi Lingkungan
- Studi iklim menggunakan isotop stabil untuk merekonstruksi perubahan iklim masa lalu dan memprediksi tren masa depan.
- Studi polusi menggunakan isotop stabil untuk mengidentifikasi sumber polutan dan melacak pergerakannya di lingkungan.
li>Studi hidrologi menggunakan isotop stabil untuk melacak pergerakan air tanah dan permukaan.
Fisika Nuklir
Dalam fisika nuklir, studi tentang isobar dan isoton telah mengarah pada pemahaman yang lebih baik tentang struktur inti atom dan reaksi nuklir.
Masa Depan
Masa depan isotop, isobar, dan isoton terlihat cerah, dengan potensi dampak yang signifikan di berbagai bidang. Penelitian berkelanjutan diharapkan mengarah pada pengembangan aplikasi baru dan pemahaman yang lebih mendalam tentang dunia fisik.
Ringkasan Akhir

Kesimpulannya, isotop, isobar, dan isoton adalah konsep fundamental dalam kimia yang memberikan pemahaman tentang sifat atom dan perbedaannya. Studi berkelanjutan tentang atom-atom ini membuka jalan bagi penemuan baru dan kemajuan teknologi, memberikan wawasan berharga tentang dunia materi yang kita tinggali.
Pertanyaan Umum (FAQ)
Apa perbedaan utama antara isotop dan isobar?
Isotop memiliki jumlah proton yang sama tetapi jumlah neutron yang berbeda, sedangkan isobar memiliki jumlah neutron yang sama tetapi jumlah proton yang berbeda.
Mengapa isoton penting dalam penelitian medis?
Isoton memiliki jumlah neutron yang sama, sehingga mereka berperilaku kimiawi dengan cara yang sama, memungkinkan penggunaan mereka sebagai pelacak dalam pencitraan medis.
Apa saja tren terbaru dalam aplikasi isotop?
Isotop stabil digunakan dalam pelacakan lingkungan, eksplorasi ruang angkasa, dan penanggalan radioaktif, sementara isotop radioaktif digunakan dalam pengobatan kanker dan pencitraan medis.