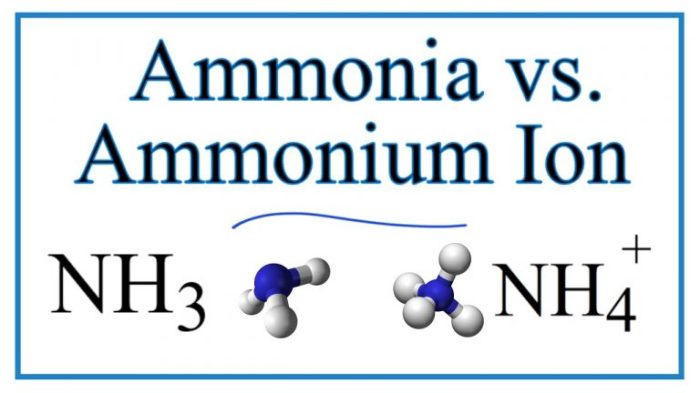
Dalam ranah kimia, amonia dan amoniak sering disalahartikan, meskipun keduanya merupakan zat yang sangat berbeda. Amonia, dengan rumus kimia NH3, adalah gas tidak berwarna dengan bau yang menyengat. Sementara itu, amoniak, dengan rumus kimia NH4+, adalah ion bermuatan positif yang terbentuk ketika amonia dilarutkan dalam air.
Perbedaan mendasar ini menghasilkan perbedaan yang mencolok dalam sifat, reaksi, dan penggunaan kedua zat tersebut. Memahami perbedaan ini sangat penting untuk aplikasi praktis dan dampak lingkungan yang terkait dengan amonia dan amoniak.
Perbedaan Definisi
Amonia dan amoniak adalah dua zat kimia yang seringkali disalahartikan sebagai hal yang sama. Namun, terdapat perbedaan penting dalam definisi keduanya.
Definisi Amonia
Amonia (NH3) adalah senyawa kimia anorganik yang terdiri dari satu atom nitrogen dan tiga atom hidrogen. Ini adalah gas tidak berwarna dengan bau yang menyengat dan dapat larut dalam air untuk membentuk larutan basa.
Definisi Amoniak
Amoniak (NH4OH) adalah senyawa kimia anorganik yang merupakan larutan amonia dalam air. Ini adalah cairan tidak berwarna dengan bau menyengat yang lebih lemah dari amonia. Amoniak adalah basa lemah yang dapat menetralkan asam.
Tabel Perbandingan Definisi
| Zat | Definisi |
|---|---|
| Amonia | Gas tidak berwarna (NH3) yang terdiri dari satu atom nitrogen dan tiga atom hidrogen |
| Amoniak | Larutan amonia dalam air (NH4OH) |
Sifat Kimia

Amonia dan amoniak memiliki sifat kimia yang berbeda, terutama dalam hal titik didih, titik leleh, dan kelarutan.
Perbedaan sifat kimia ini disebabkan oleh perbedaan struktur molekulnya. Amonia (NH3) adalah molekul polar, sedangkan amoniak (NH4+) adalah ion poliatomik.
Perbedaan Sifat Kimia
- Titik Didih: Amonia mendidih pada
-33,34 °C, sedangkan amoniak mendidih pada 100 °C. - Titik Leleh: Amonia meleleh pada
-77,73 °C, sedangkan amoniak meleleh pada 338 °C. - Kelarutan: Amonia sangat larut dalam air, sedangkan amoniak tidak larut dalam air.
Reaksi Kimia
Amonia dan amoniak bereaksi secara berbeda tergantung pada kondisi dan keberadaan katalis. Reaksi kimia yang paling umum adalah:
Reaksi Oksidasi
- Amonia dapat dioksidasi menjadi nitrogen oksida dan air dalam reaksi eksotermik:
NH 3 + 5O 2 → 4NO + 6H 2 O
- Reaksi ini digunakan dalam produksi asam nitrat dan pupuk nitrogen.
Reaksi Pembakaran
- Amonia terbakar di udara, menghasilkan nitrogen dan air:
NH 3 + 3O 2 → 2N 2 + 6H 2 O
- Reaksi ini menghasilkan panas dan cahaya, sehingga amonia dapat digunakan sebagai bahan bakar.
Reaksi Reduksi
- Amonia dapat direduksi menjadi hidrazin, yang merupakan bahan bakar roket:
NH 3 + N 2 H 4 → 3H 2 + N 2
- Reaksi ini dikatalisis oleh logam transisi seperti kobalt atau besi.
Reaksi Pembentukan Kompleks
- Amonia membentuk kompleks dengan ion logam transisi, seperti Cu2+ dan Ni2+:
[Cu(NH 3 ) 4 ] 2+ + 2NH 3 → [Cu(NH 3 ) 6 ] 2+
- Kompleks ini digunakan dalam pelapisan logam, fotografi, dan sebagai katalis.
Penggunaan
Amonia dan amoniak memiliki kegunaan yang berbeda dalam berbagai bidang industri, pertanian, dan medis.
Perbedaan utama dalam penggunaannya adalah:
- Amonia: Umumnya digunakan sebagai bahan baku untuk pupuk, bahan peledak, dan plastik.
- Amoniak: Biasanya digunakan sebagai refrigeran, pembersih, dan dalam produksi tekstil.
Industri
- Amonia: Digunakan dalam pembuatan pupuk seperti amonium nitrat, urea, dan amonium fosfat.
- Amoniak: Digunakan sebagai refrigeran dalam sistem pendingin industri dan komersial.
Pertanian
- Amonia: Digunakan sebagai pupuk nitrogen untuk tanaman.
li> Amoniak : Tidak digunakan dalam pertanian.
Medis
- Amonia : Tidak digunakan dalam pengobatan.
- Amoniak : Digunakan sebagai stimulan pernapasan dan dalam produksi obat-obatan.
Dampak Lingkungan
Amonia dan amoniak memiliki dampak lingkungan yang berbeda karena sifat dan penggunaannya yang berbeda. Penting untuk memahami dampak ini untuk meminimalkan efek negatifnya.
Dampak pada Kualitas Udara
Amonia dapat berkontribusi pada pembentukan partikulat halus (PM2,5) di atmosfer, yang dapat menyebabkan masalah pernapasan dan kardiovaskular. Amoniak, di sisi lain, dapat bereaksi dengan oksida nitrogen untuk membentuk senyawa organik volatil (VOC), yang juga berkontribusi pada polusi udara.
Dampak pada Kualitas Air
Amonia dan amoniak dapat mencemari sumber air seperti sungai, danau, dan air tanah. Amonia dapat menyebabkan eutrofikasi, yang mengarah pada pertumbuhan alga yang berlebihan dan kekurangan oksigen. Amoniak, di sisi lain, dapat beracun bagi kehidupan akuatik, terutama pada konsentrasi tinggi.
Dampak pada Kualitas Tanah
Amonia dan amoniak dapat mengubah pH tanah, yang dapat mempengaruhi ketersediaan nutrisi bagi tanaman. Amonia dapat menyebabkan alkalinisasi tanah, sementara amoniak dapat menyebabkan pengasaman. Perubahan pH ini dapat mempengaruhi pertumbuhan tanaman dan struktur komunitas mikroba tanah.
Contoh Penggunaan

Amonia dan amoniak memiliki berbagai aplikasi dalam kehidupan sehari-hari, masing-masing sesuai dengan sifat uniknya.
Berikut adalah contoh spesifik penggunaan kedua zat tersebut:
Pembersih Rumah Tangga
- Amonia encer adalah bahan umum dalam pembersih rumah tangga, seperti pembersih kaca dan lantai.
- Sifat basa amonia membantu menghilangkan kotoran dan noda dengan melarutkan minyak dan lemak.
Pupuk Pertanian
- Amoniak adalah bahan utama dalam pupuk nitrogen, yang penting untuk pertumbuhan tanaman.
- Amoniak memberikan nitrogen dalam bentuk yang dapat diserap tanaman, meningkatkan hasil panen.
Refrigeran
- Amonia adalah refrigeran yang digunakan dalam sistem pendingin, seperti lemari es dan AC.
- Sifat termodinamika amonia membuatnya cocok untuk menyerap dan melepaskan panas, sehingga menciptakan efek pendinginan.
Produksi Tekstil
- Amoniak digunakan dalam produksi tekstil untuk menghilangkan lemak dan kotoran dari serat alami seperti wol dan sutra.
- Sifat basa amonia membantu memecah minyak dan kotoran, membuat serat lebih lembut dan halus.
Produksi Farmasi
- Amonia adalah bahan baku dalam produksi obat-obatan, seperti efedrin dan pseudoefedrin.
- Sifat basa amonia membantu menetralkan asam dalam reaksi kimia yang digunakan untuk membuat obat-obatan ini.
Pemungkas

Kesimpulannya, amonia dan amoniak adalah zat yang berbeda secara signifikan dengan sifat kimia, reaksi, dan penggunaan yang berbeda. Pemahaman yang jelas tentang perbedaan ini sangat penting untuk memanfaatkan zat-zat ini secara efektif dan meminimalkan dampak lingkungannya.
Ringkasan FAQ
Apakah amoniak dan amoniak adalah zat yang sama?
Tidak, amonia (NH3) adalah gas, sedangkan amoniak (NH4+) adalah ion bermuatan positif.
Apa reaksi kimia umum yang melibatkan amonia?
Amonia bereaksi dengan asam untuk membentuk garam amonium, seperti amonium klorida.
Apa penggunaan utama amoniak?
Amoniak digunakan sebagai bahan baku untuk pupuk, bahan peledak, dan plastik.
