Perbedaan ikatan kovalen polar dan nonpolar – Dalam kimia, ikatan kovalen memegang peranan penting dalam membentuk molekul dan menentukan sifatnya. Di antara ikatan kovalen, terdapat perbedaan antara ikatan polar dan nonpolar, yang sangat mempengaruhi karakteristik dan perilaku molekul.
Artikel ini akan membahas secara mendalam perbedaan antara ikatan kovalen polar dan nonpolar, mengeksplorasi faktor-faktor yang mempengaruhi polaritas, implikasinya pada sifat molekul, dan penerapannya dalam berbagai bidang.
Pengertian Ikatan Kovalen: Perbedaan Ikatan Kovalen Polar Dan Nonpolar
Ikatan kovalen adalah jenis ikatan kimia yang terbentuk ketika dua atom berbagi satu atau lebih pasangan elektron.
Contoh ikatan kovalen adalah ikatan antara dua atom hidrogen (H 2) atau antara atom karbon dan atom oksigen (CO 2).
Ikatan kovalen berbeda dengan ikatan ionik, di mana elektron ditransfer dari satu atom ke atom lain, dan dengan ikatan logam, di mana elektron terdelokalisasi di seluruh logam.
Polaritas Ikatan Kovalen
Ikatan kovalen dapat diklasifikasikan menjadi polar dan nonpolar berdasarkan distribusi muatan elektron dalam ikatan.
- Ikatan Kovalen Nonpolar:Ketika elektron dibagikan secara merata antara kedua atom, ikatan tersebut dikatakan nonpolar. Contohnya adalah ikatan antara dua atom hidrogen (H 2).
- Ikatan Kovalen Polar:Ketika elektron dibagikan secara tidak merata antara kedua atom, ikatan tersebut dikatakan polar. Atom yang menarik elektron lebih kuat menjadi sedikit negatif, sedangkan atom yang menarik elektron lebih lemah menjadi sedikit positif. Contohnya adalah ikatan antara atom hidrogen dan atom klorin (HCl).
Elektronegativitas dan Polaritas Ikatan
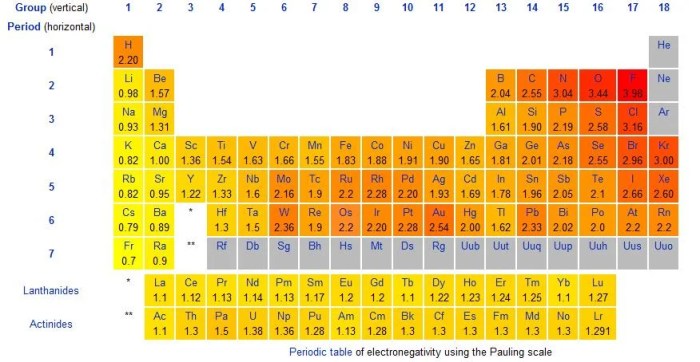
Elektronegativitas adalah ukuran kemampuan suatu atom untuk menarik elektron. Semakin tinggi elektronegativitas suatu atom, semakin kuat ia menarik elektron. Perbedaan elektronegativitas antara dua atom menentukan polaritas ikatan kovalen.
Jika perbedaan elektronegativitas antara dua atom kecil (kurang dari 0,5), ikatannya nonpolar. Jika perbedaan elektronegativitas lebih besar dari 0,5, ikatannya polar.
Ikatan Kovalen Koordinat
Ikatan kovalen koordinat adalah jenis ikatan kovalen khusus di mana kedua elektron yang dibagikan disediakan oleh satu atom.
Contoh ikatan kovalen koordinat adalah ikatan antara ion amonium (NH 4+) dan molekul air (H 2O).
Ikatan Kovalen Polar
Ikatan kovalen polar adalah jenis ikatan kovalen di mana pasangan elektron yang dibagi tidak didistribusikan secara merata antara dua atom. Ketidakmerataan distribusi ini menyebabkan pembentukan kutub positif dan negatif pada molekul.
Polaritas ikatan kovalen dipengaruhi oleh perbedaan elektronegativitas antara dua atom yang terlibat. Elektronegativitas adalah ukuran kecenderungan suatu atom untuk menarik elektron dalam ikatan kimia. Semakin besar perbedaan elektronegativitas, semakin polar ikatan kovalen.
Contoh Ikatan Kovalen Polar
- Ikatan antara hidrogen (H) dan klorin (Cl) dalam HCl
- Ikatan antara oksigen (O) dan hidrogen (H) dalam H 2O
- Ikatan antara nitrogen (N) dan hidrogen (H) dalam NH 3
Faktor-faktor yang Memengaruhi Polaritas Ikatan Kovalen
- Perbedaan Elektronegativitas:Semakin besar perbedaan elektronegativitas antara dua atom, semakin polar ikatan kovalen.
- Jenis Atom:Atom yang lebih elektronegatif cenderung menarik elektron lebih kuat, sehingga menciptakan polaritas yang lebih besar.
- Struktur Molekul:Struktur molekul dapat memengaruhi polaritas ikatan kovalen. Molekul yang memiliki ikatan kovalen polar yang mengarah ke arah yang sama akan memiliki polaritas keseluruhan yang lebih besar.
Perbedaan Ikatan Kovalen Polar dan Nonpolar

Ikatan kovalen adalah ikatan kimia yang terbentuk ketika dua atom berbagi pasangan elektron. Ikatan kovalen dapat diklasifikasikan menjadi dua jenis: polar dan nonpolar.
Dalam ikatan kovalen, elektron dibagi antara atom-atom. Jika elektron dibagi secara merata, ikatannya nonpolar. Namun, jika salah satu atom menarik elektron lebih kuat, ikatannya polar. Organ pencernaan yang bersifat sangat asam memiliki lingkungan asam yang diciptakan oleh ikatan kovalen polar dalam asam lambung.
Ikatan-ikatan ini memungkinkan proton bermuatan positif terlepas, menciptakan lingkungan yang sangat asam yang diperlukan untuk memecah makanan.
Ikatan kovalen polar terjadi ketika atom-atom yang terlibat memiliki perbedaan elektronegativitas yang signifikan. Elektronegativitas adalah ukuran seberapa kuat suatu atom menarik elektron. Perbedaan elektronegativitas menyebabkan elektron tidak terdistribusi secara merata antara kedua atom, sehingga menciptakan kutub positif dan negatif dalam ikatan.
Ikatan Kovalen Nonpolar
Ikatan kovalen nonpolar terjadi ketika atom-atom yang terlibat memiliki perbedaan elektronegativitas yang kecil. Dalam ikatan ini, elektron terdistribusi secara merata antara kedua atom, sehingga tidak ada kutub positif atau negatif yang tercipta.
Implikasi Perbedaan Ikatan Kovalen Polar dan Nonpolar
Perbedaan antara ikatan kovalen polar dan nonpolar memiliki implikasi yang signifikan terhadap sifat molekul. Molekul yang mengandung ikatan kovalen polar memiliki momen dipol, yang merupakan ukuran ketidaksimetrisan distribusi muatan dalam molekul. Momen dipol menyebabkan molekul-molekul ini memiliki sifat polar, artinya mereka memiliki kutub positif dan negatif.
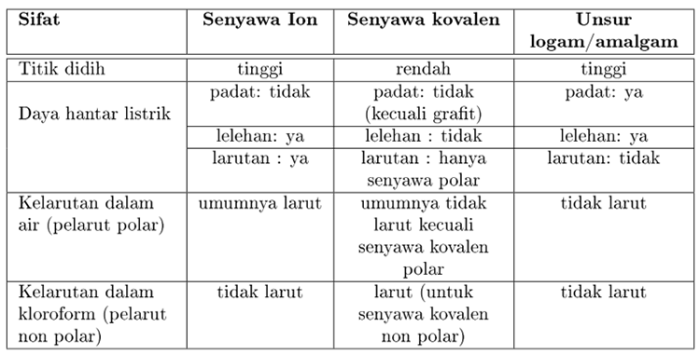
Molekul dengan ikatan kovalen nonpolar tidak memiliki momen dipol dan tidak polar. Perbedaan polaritas ini memengaruhi sifat fisik dan kimia zat. Zat yang mengandung molekul polar cenderung larut dalam pelarut polar, sedangkan zat yang mengandung molekul nonpolar cenderung larut dalam pelarut nonpolar.
Dalam kimia, ikatan kovalen dapat diklasifikasikan menjadi polar dan nonpolar berdasarkan perbedaan keelektronegatifan atom yang terlibat. Ikatan kovalen polar terjadi ketika terdapat perbedaan keelektronegatifan yang signifikan, sehingga elektron tidak terdistribusi secara merata. Sebaliknya, ikatan kovalen nonpolar terjadi ketika perbedaan keelektronegatifan sangat kecil, sehingga elektron terdistribusi secara merata.
Perbedaan ini berdampak pada sifat ikatan, dengan ikatan polar memiliki karakter ionik parsial, sementara ikatan nonpolar murni kovalen. Untuk memahami konsep ini lebih lanjut, penting untuk mengeksplorasi jelaskan pengertian akuntansi pemerintahan . Akuntansi pemerintahan merupakan sistem akuntansi yang digunakan oleh entitas pemerintah untuk mencatat dan melaporkan transaksi keuangan.
Dengan memahami perbedaan antara ikatan kovalen polar dan nonpolar, kita dapat lebih memahami prinsip-prinsip akuntansi pemerintahan, yang melibatkan pengukuran dan pelaporan transaksi keuangan yang kompleks.
Aplikasi Ikatan Kovalen

Ikatan kovalen memiliki peran penting dalam berbagai aspek kehidupan sehari-hari. Dari bahan yang kita gunakan hingga proses biologis yang terjadi di dalam tubuh kita, ikatan kovalen memainkan peran krusial.
Dalam ikatan kovalen, pasangan elektron ikatan dapat didistribusikan secara merata (nonpolar) atau tidak merata (polar). Polaritas ikatan ini dipengaruhi oleh perbedaan keelektronegatifan atom-atom yang terlibat. Sama seperti ikatan kovalen, perdagangan internasional juga dapat dipengaruhi oleh hambatan-hambatan yang diberlakukan pemerintah, seperti hambatan perdagangan internasional proteksi . Hambatan ini dapat menciptakan ketidakseimbangan dalam distribusi barang dan jasa antar negara, mirip dengan ketidakseimbangan distribusi elektron dalam ikatan kovalen polar.
Contoh Produk dan Bahan, Perbedaan ikatan kovalen polar dan nonpolar
- Air (H2O): Molekul air terdiri dari dua atom hidrogen yang terikat secara kovalen ke satu atom oksigen.
- Garam meja (NaCl):Ion natrium dan klorida terikat secara kovalen untuk membentuk kristal garam.
- Plastik:Polimer seperti polietilen dan polipropilen terbentuk melalui ikatan kovalen antara unit monomer.
Peran dalam Biologi
Ikatan kovalen sangat penting untuk kehidupan. Mereka menyusun tulang punggung DNA dan RNA, yang membawa informasi genetik.
- Protein:Asam amino terikat secara kovalen untuk membentuk rantai polipeptida, yang melipat menjadi protein dengan fungsi khusus.
- Enzim:Protein yang mengkatalisis reaksi biokimia memiliki situs aktif yang bergantung pada ikatan kovalen untuk berinteraksi dengan substrat.
Peran dalam Kimia
Ikatan kovalen membentuk dasar banyak reaksi kimia. Mereka terlibat dalam:
- Sintesis organik:Ikatan kovalen baru dibuat untuk membentuk molekul organik yang kompleks.
- Kimia anorganik:Ikatan kovalen membentuk kompleks logam dan senyawa koordinasi.
Peran dalam Industri
Ikatan kovalen digunakan dalam berbagai aplikasi industri, seperti:
- Semikonduktor:Ikatan kovalen antara atom silikon membentuk struktur kristal semikonduktor.
- Serat optik:Ikatan kovalen yang kuat dalam serat kaca memungkinkan transmisi sinyal optik jarak jauh.
Penutupan

Dengan memahami perbedaan antara ikatan kovalen polar dan nonpolar, kita dapat memperoleh pemahaman yang lebih komprehensif tentang sifat kimiawi zat, memprediksi perilaku molekul, dan memanfaatkan ikatan ini dalam berbagai aplikasi di bidang sains dan industri.
Pertanyaan dan Jawaban
Apa itu ikatan kovalen?
Ikatan kovalen adalah ikatan kimia yang terbentuk ketika dua atom berbagi elektron untuk mencapai konfigurasi elektron yang stabil.
Apa perbedaan utama antara ikatan kovalen polar dan nonpolar?
Ikatan kovalen polar terjadi ketika elektron tidak dibagi sama rata antara kedua atom, sedangkan ikatan kovalen nonpolar terjadi ketika elektron dibagi sama rata.
Apa saja faktor yang mempengaruhi polaritas ikatan kovalen?
Perbedaan elektronegativitas antara atom yang terlibat, ukuran atom, dan geometri molekul dapat mempengaruhi polaritas ikatan kovalen.
